2024年1月22日,国家药监局器审中心发布了关于公开征求《肿瘤筛查用体外诊断试剂临床评价注册审查指导原则(征求意见稿)》指导原则意见的通知。
2025年8月21日,通告落地:
相比于征求意见稿,变化非常大,下面我们挑几个点看对于试剂盒开发商的产品布局有哪些利好。
其一,提倡积极预防,推进早发现早诊断

其二,删除了对于“其他癌种”的描述,增加了申报的可能性
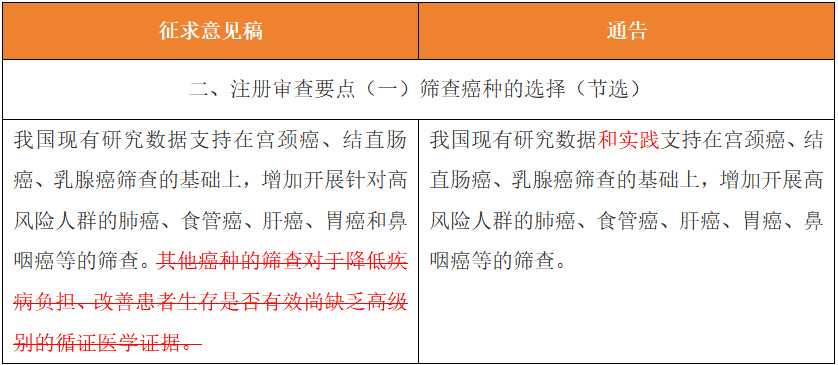
其三,解绑“符合流行病学的要求”,监管框架明确允许性能指标差异化

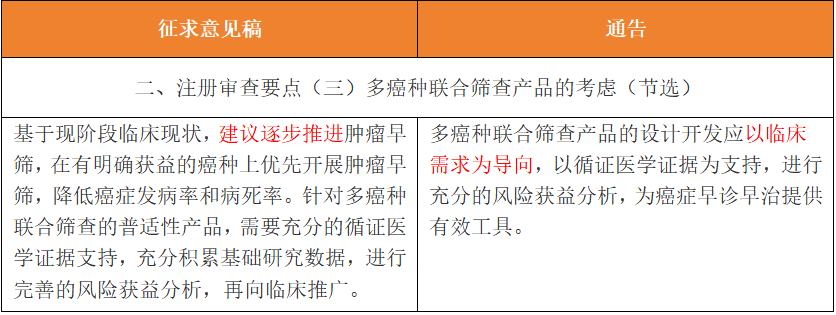
其四,多癌种联合筛查产品从逐步推进到以临床需求为导向的跨越,给了产品布局更多的机会
癌症是全球重大公共卫生挑战,筛查是降低死亡率的关键手段。近岸蛋白凭借自主核心技术平台,开发并量产多款高性能分子酶及诊断级试剂原料,赋能诊断企业加速产品研发与产业化,携手共建高效协同的行业生态,助力中国精准医疗高质量发展。明星产品——DNA甲基化检测预混液通过主文档登记备案,助力客户申报流程更快捷。
所有者名称:苏州近岸蛋白质科技股份有限公司
主文档登记事项名称:DNA甲基化检测预混液主文档
主文档登记号:M2023150-000
登记/更新时间:2023/12/8
部分产品性能展示
优异的扩增性能
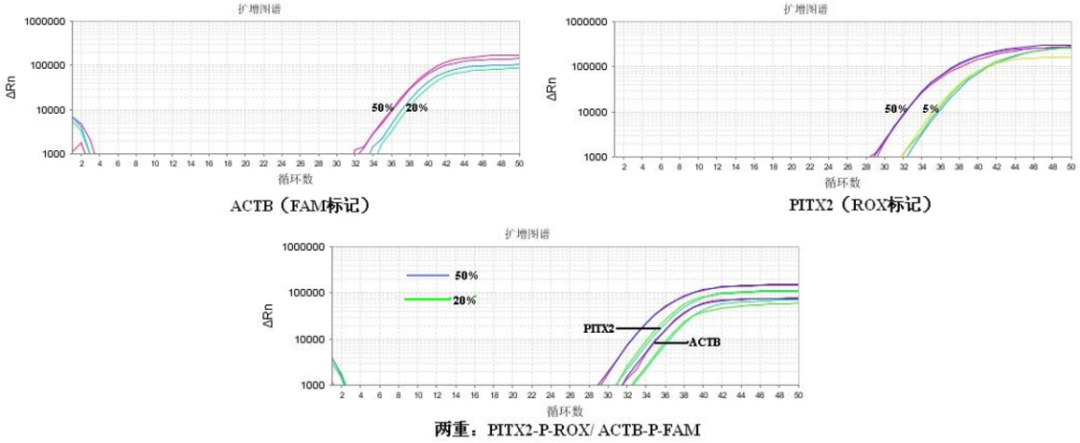
图1. 不同甲基化水平的DNA样本扩增
可稳定检测到低至5%的甲基化水平
稳定性好
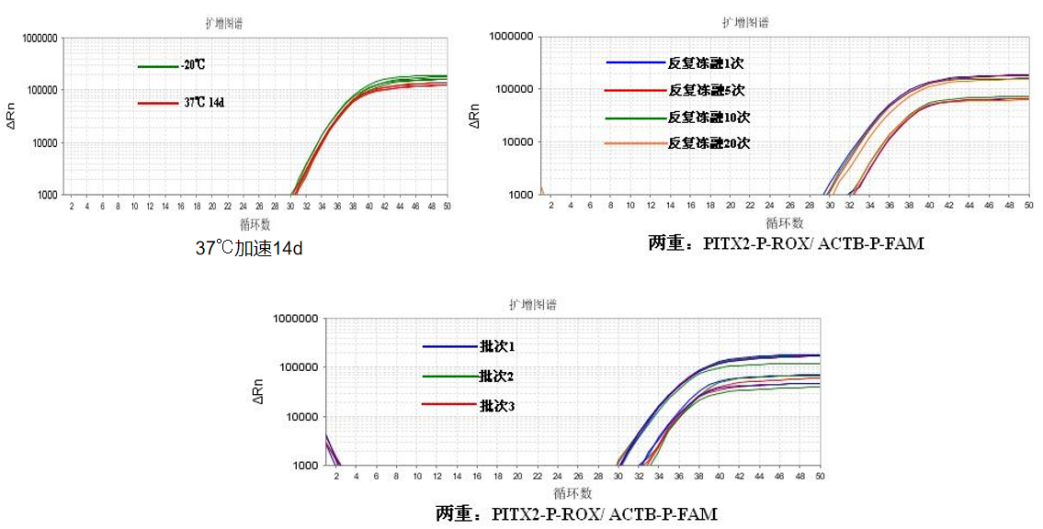
图2. 热加速稳定性和反复冻融测试
37℃加速14d和反复冻融20次的检测性能跟-20℃一致,三批次差异不显著
优化升级
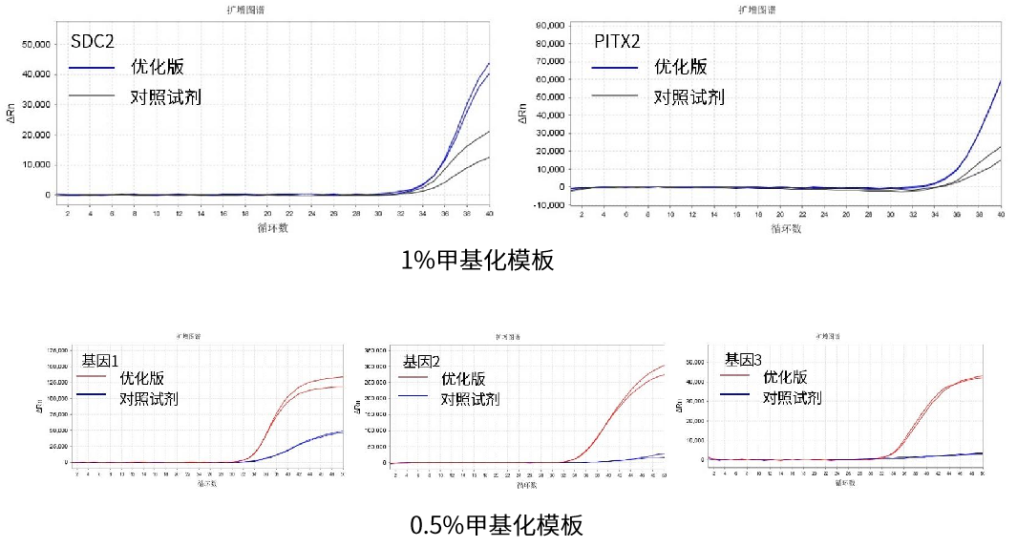
图3. 优化版(E498)测试
优化版的检测甲基化水平更灵敏,荧光信号更强
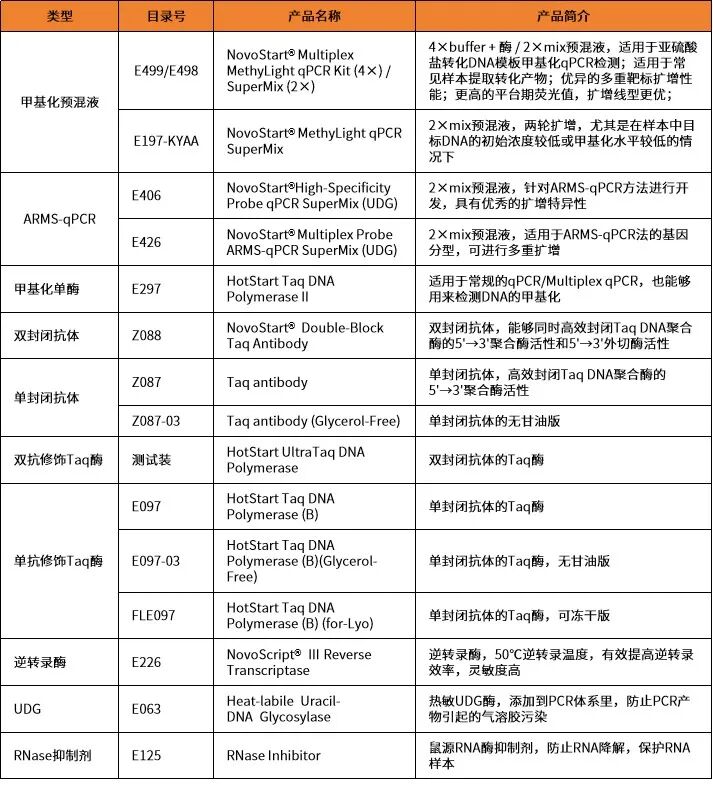
相关产品
参考文献
[1]WHO 结直肠癌
[2]国家药监局器审中心公开征求《肿瘤筛查用体外诊断试剂临床评价注册审查指导原则(征求意见稿)》意见的通知
[3]国家药监局器审中心关于发布癌症筛查体外诊断试剂临床评价注册审查指导原则等4项指导原则的通告(2025年第16号)
